Velocidad de una reacción
LA VELOCIDAD DE UNA REACCIÓN QUÍMICA
La velocidad de una reacción describe que tan rápido se consume los reactivos y se forman los productos. La cinética química se dedica al estudio de la velocidad de las reacciones químicas, los factores que afectan la velocidad y los mecanismos por los cuales ocurren las reacciones.
Nuestra experiencia nos dice que reacciones distintas tienen lugar a velocidades diferentes; las reacciones químicas como quemar metano, y la de quemar isooctano, proceden con suma rapidez, a veces de formas explosiva.
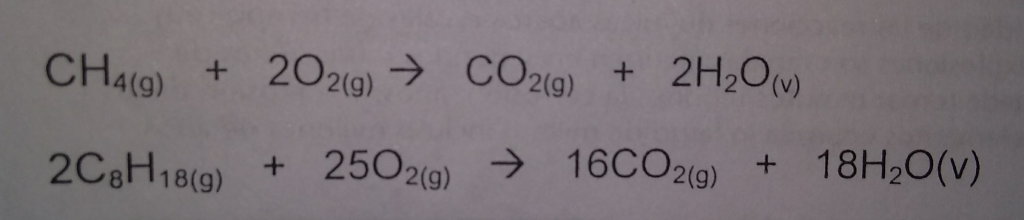
Por otra parte el enmohecimiento del hierro tiene lugar a mucha lentitud.
Comprender y controlar la velocidad de las reacciones resulta muy importante en casi todas las áreas, en todo sistema vivo, un número enorme de reacciones debe interconectarse con suavidad. Las plantas y animales usan múltiples maneras, de proveer los materiales de una reacción con la velocidad y cantidad necesarias para reacciones subsecuentes. Las enfermedades suelen perturbar el control normal de la velocidad de las reacciones. En la conservación de los alimentos por refrigeración se intenta ralentizar la velocidad de las reacciones de putrefacción indeseables. Igualmente los químicos desean establecer las condiciones para producir materiales a velocidad útil y económica en tanto hacen más lentas las reacciones secundarias indeseables y evitan la velocidad peligrosamente alta que pudiera generar explosiones.
Termodinámicamente se puede conocer si la reacción es o no espontánea y que cantidad de energía se absorbe o libera. La velocidad a la cual procede la reacción dicta la cinética, aunque la misma sea espontanea en términos termodinámicos, esta podría no ocurrir a velocidad medible.
Simulación






Comentarios recientes