Guía No.8. La constante de equilibrio de un ácido débil.
LA CONSTANTE DE EQUILIBRIO DE UN ÁCIDO DÉBIL
OBJETIVO
Determinar experimentalmente la constante de equilibrio, Ka para la disociación de un ácido débil.
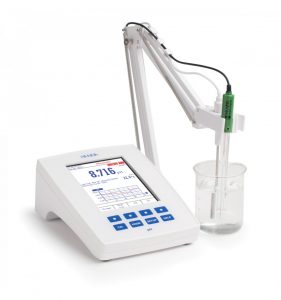
PH-METRO
Consta esencialmente de dos partes: los electrodos y el potenciómetro propiamente dicho. Los electrodos más utilizados son, en general, el de calomelanos, como electrodo de referencia y el de vidrio como electrodo del tipo llamado combinado, que lleva en sí incluidos tanto el electrodo de referencia como el de medida,. Esta simplificación supone sensibles ventajas, ya que, al sólo precisar la introducción en la solución problema de un electrodo, permite, entre otras cosas, la medición del pH en volúmenes muy pequeños. El potenciómetro mide la diferencia de potencial que se establece entre los dos electrodos y nos indica directamente el pH de la solución.
Calibración del pH-metro





1. Una Ke >>1 favorece los reactivos o productos?
2. ¿Por qué se omite la concentración de agua en el equilibrio de soluciones acuosas?
1. Favorece los productos.
2. Porque el agua es un líquido puro, y por esto no tiene cambios significativos. Por ende no influye en el cambio de equilibrio.
Ángela Ocampo Rodas, Miller Londoño
Veronica valencia y juan diego correa
1 Una constante de equilibrio (K) mayor que 1 favorece a los productos
2 La concentración de agua se omite en el equilibrio de soluciones acuosas porque es muy grande y prácticamente constante, por lo que no afecta significativamente el equilibrio.
1- El equilibrio favorece mas a los productos que a los reactivos
2- Porque es prácticamente constante en comparación con los solutos y no afecta significativamente el cociente de las concentraciones.
Danna Isabella Quiroga- Laura Camila Calderón
1. Una Ke >> 1 favorece a los productos.
2.La concentración del agua se omite debido a que esta es el solvente y su concentración es prácticamente constante en reacciones acuosas.
– Juan Manuel Gómez Montoya
– Luis David Serna Loaiza